Как слепить молекулы из пластилина.
Многие школьники не любят химию и считают ее скучным предметом. Многим этот предмет дается с трудом. Но ее изучение может быть интересным и познавательным, если подойти к процессу творчески и показать все наглядно.
Предлагаем вам подробное руководство по лепке молекул из пластилина.
Перед изготовлением молекул нам нужно заранее определиться с тем, какие химические формулы будем использовать. В нашем случае это этан, этилен, метилен. Нам понадобятся: пластилин контрастных цветов (в нашем случае – красный и синий) и немного зеленого пластилина, спички (зубочистки).


1. Из красного пластилина скатываем 4 шарика диаметром около 2 см (атомы углерода). Затем из синего пластилина скатываем 8 шариков поменьше, диаметром около сантиметра (атомы водорода).


2. Берем 1 красный шарик и вставляем в него 4 спички (или зубочистки)так, как показано на рисунке.


3. Берем 4 синих шарика и надеваем их на свободные концы вставленных в красный шарик спичек. Получилась молекула природного газа.


4. Повторяем шаг №3 и получаем две молекулы для следующего химического вещества.


5. Сделанные молекулы нужно соединить между собой спичкой для того, чтобы получилась молекула этана.


6. Также можно создать молекулу с двойной связью — этилен. Для этого, из каждой молекулы, полученной при выполнении шага № 3 вынимаем по 1 спичке с надетым на нее синим шариком и соединяем детали между собой двумя спичками.




7. Берем красный шарик и 2 синих и соединяем их между собой двумя спичками так, чтобы получилась цепочка: синий – 2 спички – красный – 2 спички – синий. У нас получилась еще одна молекула с двойной связью – метилен.


8. Берем оставшиеся шарики: красный и 2 синих и соединяем их спичками между собой как показано на рисунке. Затем скатываем из зеленого пластилина 2 маленьких шарика и прикрепляем к нашей молекуле. У нас получилась молекула с двумя отрицательно заряженными электронами.


Изучение химии станет интереснее, а у вашего ребенка появится интерес к предмету.


Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
moy-karapuzik.ru
[20.09.2013 18:14] Номер задачи на нашем сайте: 1437 ГДЗ из решебника: Тема: Нашли ошибку? Сообщите в комментариях (внизу страницы)
| Source: bambookes.ru|||
kak.radiomoon.ru
Поурочный план лабораторной работы по теме: «Изготовление моделей молекул углеводородов»
Составить шаростержневую модель молекулы метана:
— сделать из черного пластилина один шарик, который будет символизировать атом углерода, и из белого пластилина сделать четыре шарика, которые будут символизировать атомы водорода. Причем диаметр черного шарика должен превышать диаметр белых шариков в 1,5 раза.
— на черном шарике (атом углерода) наметьте четыре равноудаленные друг от друга точки и вставьте в них палочки, к концам палочек присоедините четыре белых шарика (атомы водорода).
Составить шаростержневую модель молекулы трихлорметана:
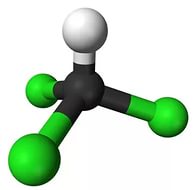
— исходя из модели молекулы метана, составьте модель молекулы трихлорметана.
— сделать из синего пластилина три шарика, которые будут символизировать атом хлора. Причем диаметр синих шариков должен превышать диаметр белых шариков в 2 раза.
— отнимите от модели молекулы метана три шарика белого цвета (символ атома водорода) и на освободившиеся места прикрепите синие шарики (символ атома хлора).
Составить шаростержневую модель молекулы этана:
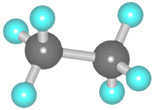
— сделать из черного пластилина два шарика, которые будут символизировать атом углерода, и из белого пластилина сделать шесть шариков, которые будут символизировать атомы водорода. Причем диаметр черных шариков должен превышать диаметр белых шариков в 1,5 раза.
— соедините между собой палочкой шарики черного цвета.
— на каждом черном шарике (атом углерода) наметьте три равноудаленные друг от друга точки и вставьте в них палочки, к концам палочек присоедините белый шарик (атомы водорода).
Составить шаростержневую модель молекулы хлорэтана:
— исходя из модели молекулы этана, составьте модель молекулы хлорэтана.
— сделать из синего пластилина шарик, которые будут символизировать атом хлора. Причем диаметр синего шарика должен превышать диаметр белых шариков в 2 раза.
— отнимите от модели молекулы этана один шарик белого цвета (символ атома водорода) и на освободившееся место прикрепите синий шарик (символ атома хлора).
Составить шаростержневую модель молекулы бутана:

— сделать из черного пластилина четыре шарика, которые будут символизировать атом углерода, и из белого пластилина сделать десять шариков, которые будут символизировать атомы водорода. Причем диаметр черных шариков должен превышать диаметр белых шариков в 1,5 раза.
— соедините между собой палочками шарики черного цвета.
— на первый и четвертый черный шарик (атом углерода) наметьте три равноудаленные друг от друга точки и вставьте в них палочки, к концам палочек присоедините белый шарик (атомы водорода). Ко второму и третьему черному шарику вставить по две палочки, к концам палочек присоедините белый шарик (атомы водорода).
Выводы по лабораторной работе: _______________________________________________________.
Контрольные вопросы по защите лабораторной работе:
Какие существуют способы моделирования молекул органических соединений?
Какие положения теории химического строения органических соединений учитывались при составлении моделей молекул углеводородов?
Записать название соединений их структурные формулы. С6Н14, С7Н16. Составить изомеры этих соединений, назвать их.
infourok.ru
Инструкция к практической работе: «Изготовление моделей углеводородов»
Цель работы: научиться составлять модели молекул углеводородов, записывать сокращённые структурные формулы и называть их по международной номенклатуре, составлять структурные формулы углеводородов по названию.
Оборудование; шарики из пластилина, имитирующие атомы углерода и водорода, спички, инструкции к работе, дощечки для работы с пластилином.
Инструктаж по технике безопасности.
1.Работать строго по инструкции.
2.Пластилиновые шарики и спички использовать только для составления моделей углеводородов.
3.Модели собирать над дощечкой для работы с пластилином.
5.После проверки учителем изготовленных моделей молекул, модели разобрать, шарики и спички положить в соответствующие коробочки и сдать лаборанту.
6.Вымыть руки с мылом.
7.Приступить к выполнению теоретического задания в тетрадях для практических работ.
Указание к работе. Работа выполняется по вариантам. Задание 1 общее для 1 и 2 вариантов. Учащиеся работают в парах.
Задание 1. Соберите модели молекул метана, пропана, бутана.
Что общего в строении молекул этих веществ, в чем различие? Чем объясняется зигзагообразное строение углеродной цепи в молекулах пропана и бутана? Какова величина угла в зигзагообразном отрезке углеродной цепи? Продемонстрируйте на моделях молекул этана и пропана возможность свободного вращения углеводородных радикалов относительно друг друга (конформация) и образования в результате этого огромного числа пространственных изомеров. Почему нельзя выделить эти изомеры? Как называется химическая связь, образованная в результате перекрывания электронных облаков вдоль линии, связывающей центры атомов?
Выполнение опыта.
1. Возьмите шарик, который условно будет изображать атом углерода, и четыре стержня (или спички), которые будут изображать связи С—Н. Объясните, почему химические связи располагаются вокруг атома углерода под углом 109°28′ относительно друг друга. Расположите четыре стержня под указанным углом между ними.
2. Мысленно или при помощи нити соедините центры ядер атомов водорода (свободные концы стержней) друг с другом. Изображение какой геометрической фигуры вы получили?
3. На свободные концы стержней прикрепите (наколите) четыре шарика. Такая модель молекулы метана называется шаростержневой моделью.
Аналогичные модели молекул, в которой детали, изображающие атомы элементов, выполняются в соответствующем масштабе, называются масштабными.
Вариант 1
Задание 2.Соберите модель молекулы С3Н6. Сколько спичек вы расположили между атомами углерода? Как называется эта связь? К какому классу соединений принадлежит этот углеводород? Какой тип гибридизации атомов углерода? Валентный угол? Возможно ли свободное вращение атомов при двойной связи? Запишите общую формулу углеводородов этого класса. Какие виды изомерии характерны для них?
Задание 3.Назовите вещества
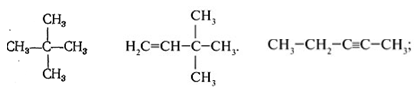
Задание 4.Составьте структурные формулы:
а) 2-метилбутен-2 напишите его изомер;
б) 3,4-диметилпентин-1.
Вариант 2.
Задание 2. Соберите модель молекулы С3Н4. Сколько спичек вы расположили между атомами углерода? Как называется эта связь? К какому классу соединений принадлежит этот углеводород? Какой тип гибридизации атомов углерода? Валентный угол? Возможно л и свободное вращение атомов при тройной связи? Запишите общую формулу углеводородов этого класса. Какие виды изомерии характерны для них?
Задание 3.Назовите вещества:
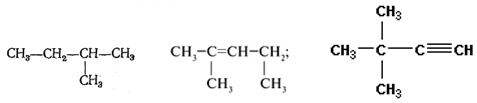
Задание 4.Составьте структурные формулы:
а) бутен-2, напишите его изомер;
б) 3,3 — диметилпентин-1.
infourok.ru
ПО «Mozaik». 3D-модели по химии
В составе программного обеспечения «Mozaik» имеются 3D-модели для изучения школьного курса химии. На 3D-моделях наглядно представлены различные химические объекты — атомы, молекулы, а также механизмы реакций.3D-модели по химии размещены в нескольких меню: неорганическая химия, общая химия, органическая химия.


Ниже представлен список. Сами 3D-модели по химии можно посмотреть на сайте mozaweb.com (в ознакомительном режиме имеются ограничения по количеству просматриваемых 3D-моделей в сутки).
Азот

Азотистая кислота
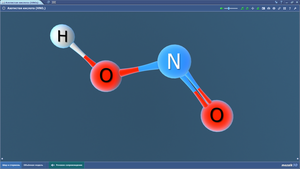
Азотная кислота

Аланин

Алканы

Алмаз

Альфа-D-глюкоза
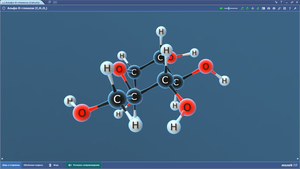
Амилоза

Аминокислоты

Аммиак

Анилин
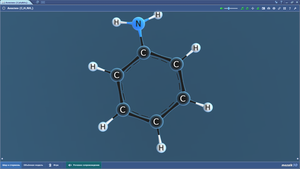
Аргинин
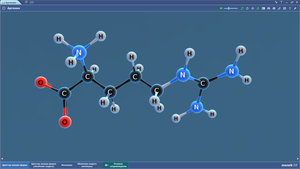
Аспарагин
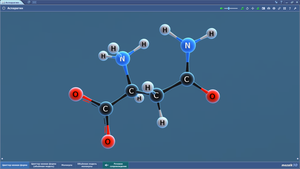
Аспарагиновая кислота

Атомные орбитали кальция

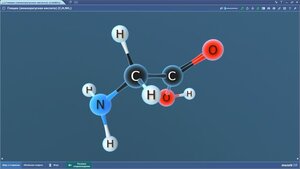
Ацетальдегид (этаналь)
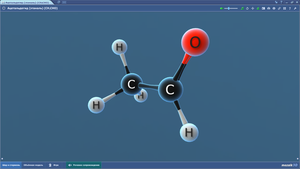
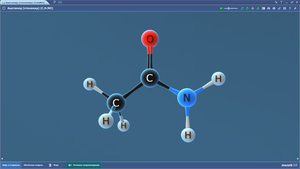
Ацетамид
Ацетилен
Ацетон

Белый фосфор

Бензойная кислота

Бензол
Бета-D-глюкоза

Бета-D-рибоза

Бета-D-фруктоза

Бром
Бромид серебра
Бромоводород

Бромфторхлорметан
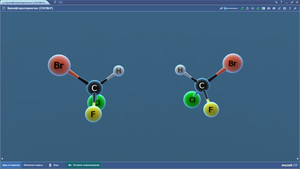
Бутан

Бутадиен-1,3
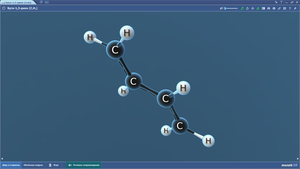
Бутен-1

Валин

Взаимодействие аммиака с хлороводородом
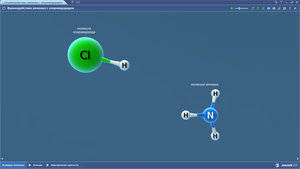
Винилхлорид

Вода
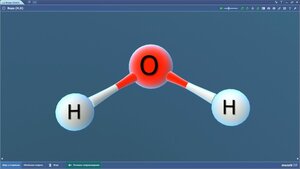
Водород

Вторичная структура белков

Гексагональная плотноупакованная решетка

Гексан

Гемоглобин

Гидрат метана
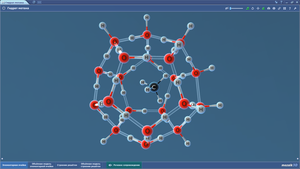
Гидрат-ион

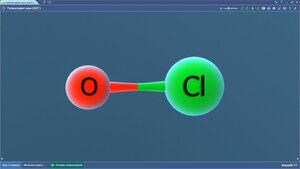
Гипохлорит-ион
Гистидин

Глицеральдегид

Глицерин
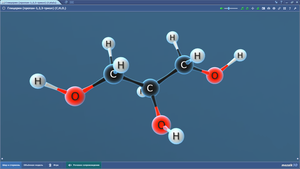
Глицилглицин
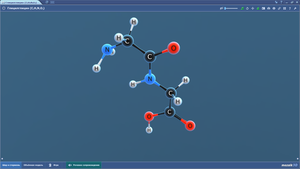
Глицин
Глутамин

Глутаминовая кислота

Гранецентрированная кубическая решетка

Графит

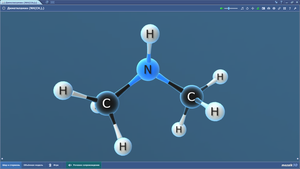
Диметиламин
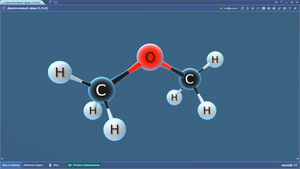
Диметиловый эфир
Диоксид азота

Диоксид кремния

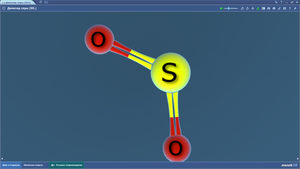
Диоксид серы
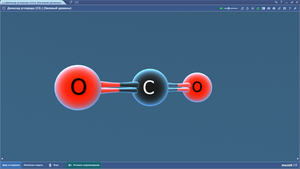
Диоксид углерода
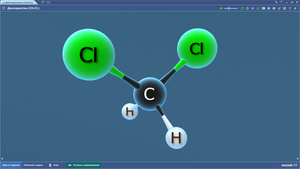
Дихлорметан
Диэтиловый эфир

ДНК

Задания по теме МОЛЕКУЛЫ. Полярность
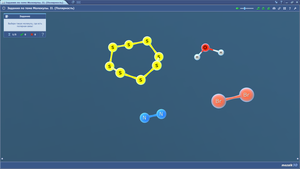
Задания по теме МОЛЕКУЛЫ. Сложные ионы

Задания по теме МОЛЕКУЛЫ. Углеводороды

Задания по теме МОЛЕКУЛЫ. Кислородсодержащие органические соединения
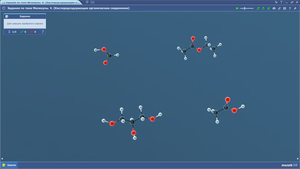
Задания по теме МОЛЕКУЛЫ. Углеводы

Задания по теме МОЛЕКУЛЫ. Азотсодержащие органические соединения
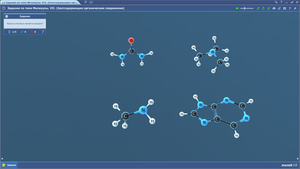
Задания по теме МОЛЕКУЛЫ. Связи в молекулах

Замыкание в цикл молекулы глюкозы

Изменения агрегатного состояния

Изобутан
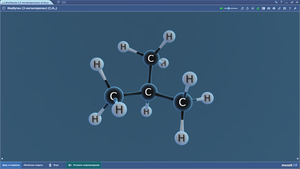
Изолейцин
melnik-a.livejournal.com
Молекула воды из пластилина: фото
[h3]
Молекула воды[/h3]
С водой связана вся жизнь человека – от самого зарождения и до смерти. Вода – это одно из самых первых веществ, которое начинает изучать маленький исследователь – в ванне, луже и даже на кухонном столе. Ее уникальные свойства испаряться, замерзать, таять (плавиться) привлекает умы деток постарше.
Но о том, почему так происходит и из чего состоит хорошо известная вода – узнается только в старших классах школы. Однако мы склонны считать, что не стоит ждать пока познавательный интерес к этому уникальному по своим свойствам веществу начнет угасать. Ведь даже старшему дошкольнику доступны к пониманию понятия атом и молекула, тем более если их модели слепить своими собственными руками, опираясь на научные данные (с помощью взрослых).

Моделируем молекулу из пластилина
Для того чтобы смоделировать молекулу воды потребуется пластилин двух цветов и спички.
Молекула воды состоит из атомов двух элементов – водорода и кислорода
.
В Периодической системе Д.И. Менделеева эти элементы расположены под номером 1 и 8. Этот номер называется порядковым. Ниже в этой же клеточке есть еще одно число (с несколькими цифрами после запятой) – это относительная атомная масса элемента.
Для большей наглядности на кухонных электронных весах можно измерить массу пластилиновых шариков, демонстрирующих атомы этих элементов.
[h3]
Кислорода:[/h3]

и
водорода:

Заметим, что масса получившихся «атомов» по сравнению с настоящими увеличена в 1000 000 000 000 000 000 000 000 (10 в 24 степени) раз.
По размеру получилось примерно, что атом кислорода «похож» со сливу, а атом водорода – на горошину.
В молекуле воды два атома водорода и один атом кислорода располагаются достаточно близко друг к другу, но под определенным углом. Если обозначить «центр» атома кислорода точкой, приложить к нему центральную метку транспортира, то атомы водорода будут находиться по отношению друг к другу под углом 104 градуса.

В итоге у нас получилась вот такая модель молекулы воды:









vilingstore.net
Опыт № 11/12. Изготовление моделей молекул органических соединений
Оборудование. Наборы разного цвета шаров и стержней.
А. Изготовление моделей углеводородов и их галогенопроизводных
Задания. 1—5. Соберите шаростержневые модели молекулы метана и его гомологов.
6—7. Соберите шаростержневые модели молекул дихлор-метана и дихлорэтана.
Выполнение опыта
1. Возьмите шарик, который условно будет изображать атом углерода, и четыре стержня (или спички), которые будут изображать связи С—Н. Объясните, почему химические связи располагаются вокруг атома углерода под углом 109°28′ относительно друг друга. Расположите четыре стержня под указанным углом между ними.
2. Мысленно или при помощи нити соедините центры ядер атомов водорода (свободные концы стержней) друг с другом. Изображение какой геометрической фигуры вы получили?
3. На свободные концы стержней прикрепите (наколите) четыре шарика. Такая модель молекулы метана называется шаростержневой моделью.
Аналогичные модели молекул, в которой детали, изображающие атомы элементов, выполняются в соответствующем масштабе, называются масштабными.
4. Соберите шаростержневые модели молекул метана, этана, пропана, бутана.
Что общего в строении молекул этих веществ, в чем различие? Чем объясняется зигзагообразное строение углеродной цепи в молекулах пропана и бутана? Какова величина угла в зигзагообразном отрезке углеродной цепи? Продемонстрируйте на моделях молекул этана и пропана возможность свободного вращения углеводородных радикалов относительно друг друга (конформация) и образования в результате этого огромного числа пространственных изомеров. Почему нельзя выделить эти изомеры?
5. Изготовьте шаростержневые модели н-бутана и н-пентана. С помощью моделей покажите возможный переход парафинов в циклопарафины и наоборот. Сохраняется ли размер валентных углов в углеродной цепи парафинов при превращении их в циклопарафины?
6. Изготовьте шаростержневые модели молекул метана и четырех молекул хлора. С помощью этих моделей продемонстрируйте поэтапное замещение атомов водорода в метане на атомы хлора с образованием хлороводорода и соответствующих галогенопроизводных метана.
7. Соберите шаростержневые модели молекул дихлорметана и дихлорэтана. Имеются ли изомеры у этих галогенопроизводных? Если да, то покажите их с помощью моделей, назовите их.
Б. Изготовление моделей молекул метиламина и диметиламина
Выполнение опыта
1. Используя приемы, описанные выше, соберите шаростержневые модели молекул аммиака и метана. Удалите по одному атому из каждой молекулы и остатки соедините свободными валентностями. Получилась модель молекулы метиламина. Сделайте вывод, что представляет собой это соединение по отношению к аммиаку и метану.
2. Соберите шаростержневую модель молекулы диметиламина. Что представляет собой это соединение по отношению к аммиаку?
Оборудование. Наборы разного цвета шаров и стержней.
А. Изготовление моделей углеводородов и их галогенопроизводных
Задания. 1—5. Соберите шаростержневые модели молекулы метана и его гомологов.
6—7. Соберите шаростержневые модели молекул дихлор-метана и дихлорэтана.
Выполнение опыта
1. Возьмите шарик, который условно будет изображать атом углерода, и четыре стержня (или спички), которые будут изображать связи С—Н. Объясните, почему химические связи располагаются вокруг атома углерода под углом 109°28′ относительно друг друга. Расположите четыре стержня под указанным углом между ними.
2. Мысленно или при помощи нити соедините центры ядер атомов водорода (свободные концы стержней) друг с другом. Изображение какой геометрической фигуры вы получили?
3. На свободные концы стержней прикрепите (наколите) четыре шарика. Такая модель молекулы метана называется шаростержневой моделью.
Аналогичные модели молекул, в которой детали, изображающие атомы элементов, выполняются в соответствующем масштабе, называются масштабными.
4. Соберите шаростержневые модели молекул метана, этана, пропана, бутана.
Что общего в строении молекул этих веществ, в чем различие? Чем объясняется зигзагообразное строение углеродной цепи в молекулах пропана и бутана? Какова величина угла в зигзагообразном отрезке углеродной цепи? Продемонстрируйте на моделях молекул этана и пропана возможность свободного вращения углеводородных радикалов относительно друг друга (конформация) и образования в результате этого огромного числа пространственных изомеров. Почему нельзя выделить эти изомеры?
5. Изготовьте шаростержневые модели н-бутана и н-пентана. С помощью моделей покажите возможный переход парафинов в циклопарафины и наоборот. Сохраняется ли размер валентных углов в углеродной цепи парафинов при превращении их в циклопарафины?
6. Изготовьте шаростержневые модели молекул метана и четырех молекул хлора. С помощью этих моделей продемонстрируйте поэтапное замещение атомов водорода в метане на атомы хлора с образованием хлороводорода и соответствующих галогенопроизводных метана.
7. Соберите шаростержневые модели молекул дихлорметана и дихлорэтана. Имеются ли изомеры у этих галогенопроизводных? Если да, то покажите их с помощью моделей, назовите их.
А. 1, 2, 3.
Потому, что этот угол (109°28′) наиболее выгоден для молекулы, получается симметричная структура: атомы и равно отдалены друг от друга и находятся на одинаковом расстоянии от атома С. Атомы водорода образуют тетраэдр, причем атом C расположен в центре.
4. Пространственное строение не изменилось.
5.
Общее: углы между связями одинаковы для разных молекул (109°28′). Зигзагообразное строение углеродной связи объясняется углом (109°28′) и способностью свободно вращаться. Пространственные изомеры нельзя выделить потому, что углеводородные радикалы вращаются свободно относительно друг друга.
6. Размер валентных углов сохраняется.
7. 8.
2.
5terka.com
